전 세계 시험군 3990명 모집해 투약 예정
연간 수억회 생산… 정부 선구매는 안 해
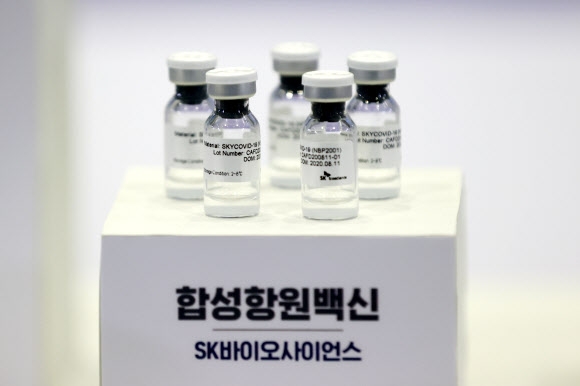
연합뉴스
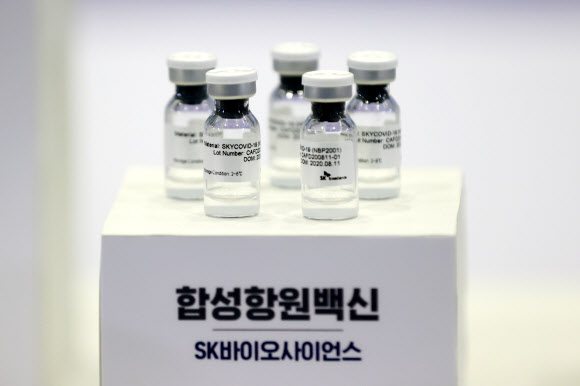
GBP510.
연합뉴스
연합뉴스
10일 식품의약품안전처에 따르면 ‘비교 임상’은 GBP510과 국내에서 이미 접종 중인 아스트라제네카(AZ)를 비교해 유효성과 안전성을 확인하는 방식이다. 일부 참여자(18세 이상 3990명)에게는 GBP510 백신을 투여하고, 다른 참여자(990명)에게는 아스트라제네카를 투여한 뒤 GBP510 투여군에 아스트라제네카 정도의 면역이 생기면 예방효과를 인정하는 식이다. 김강립 식약처장은 “(전 세계적으로) 백신 접종률이 높아 (수만명의 시험 대상자가 필요한) 전통적인 임상 방식은 하기 어려운 상황”이라고 비교 임상 도입 이유를 밝혔다.
당국은 임상시험 참여자를 최대한 빠르게 모집할 계획이다. 김 처장은 “승인 이후에 신속하게 임상시험 참여자들을 모집하는 것이 매우 중요한 과제”라면서 “이미 운영 중인 범정부 코로나19 백신 치료제 임상시험지원 태스크포스(TF)를 통해 국내외의 임상시험 대상자를 모집하는 방안을 지원하겠다”고 밝혔다. 식약처는 빠른 3상 진행을 위해 전체 임상 대상자의 10%는 국내에서 모집하도록 권고한 바 있다.
식약처의 정식 허가 심사는 내년 1분기(1~3월)에 진행될 것으로 보인다. 그간 국내외 치료제와 해외 백신의 허가 심사 기간이 최대 40일이었다는 점을 고려할 때 3월에 심사 절차에 돌입해도 상반기 내에는 백신의 정식 출시가 가능하다. 김 처장은 “우리의 목표는 가장 빠른 시간 안에 임상시험이 종료되고, 그 결과를 확인해 식약처가 허가 절차를 시작하는 것”이라고 밝혔다. 백신이 델타 변이를 포함한 주요 변이 바이러스에 어떤 효과를 보이는지도 조만간 분석이 진행될 예정이다. 향후 GBP510이 상용화되면 국내 제약사인 SK바이오사이언스는 백신 공장인 경북 안동 L하우스를 통해 연간 수억회 물량의 대규모 생산을 할 것으로 알려졌다. 다만 당국은 “선구매 계약은 아직 없다”고 밝혔다.
2021-08-11 3면
Copyright ⓒ 서울신문. All rights reserved. 무단 전재-재배포, AI 학습 및 활용 금지